Un service dédié aux
maladies neurodégénératives (MND)
Avec son savoir-faire unique de solubilisation et de stabilisation d’oligomères (AβO, αSO et TauO), ETAP-Lab propose un nouveau service de pharmacologie de criblage in vitro et in vivo dans le domaine de l’évaluation des maladies neurodégénératives protéopathiques.

Un savoir-faire unique et exclusif
ETAP-Lab dispose d’un savoir-faire unique pour produire et stabiliser des agrégats d’oligomères à partir de leurs monomères humains. Les préparations oligomères sont parfaitement caractérisées, tant au niveau physico-chimique qu’en terme de neurotoxicité.
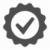
Modèles in vitro et in vivo fiables
Tous les modèles proposés sont hautement reproductibles et validés avec des molécules de référence. ETAP-Lab garantit la validité de chaque test, en utilisant des contrôles internes quantifiables. Nous sommes également certifiés ISO 9001:v2015.

Expertise et pertinence scientifique
Nos modèles sont basés sur des données scientifiques récentes démontrant l’implication des oligomères dans les premiers stades des maladies neurodégénératives. Grâce à notre équipe de neurobiologistes et de pharmacologues, nous sommes en mesure d’offrir un accompagnement scientifique de haut niveau.
They trust ETAP-Lab
Merci beaucoup pour vos services professionnels dans les études neurodégénératives in vitro. Nous collaborons avec ETAP-Lab depuis quelques années. Vous avez fourni vos services de manière professionnelle dans les délais impartis avec un haut niveau de qualité. De plus, vous avez été très proactifs pour résoudre les questions techniques. Ce fut un grand plaisir de travailler avec vous et nous sommes impatients de construire une relation à long terme avec vous ! (Traduit de l’anglais)
Dr. Yuhong Dong, CSO & Co-fondateur, SunRegen Healthcare AG
Oligomer-based in vitro models
of NDD A relevant paradigm for your drug screening
Notre service d’évaluation de l’efficacité de molécules actives vous permet maintenant de tester et de sélectionner vos composés innovants dans des modèles basés sur les dernières avancées dans la compréhension des mécanismes sous-jacents aux maladies neurodégénératives.
En effet, depuis plusieurs années, les preuves s’accumulent sur l’implication des oligomères β-amyloïde et tau pour la maladie d’Alzheimer et alpha-synucléine pour la maladie de Parkinson. Plusieurs études cliniques en cours ciblant ces oligomères montrent aujourd’hui des résultats encourageants, et pourraient à terme déboucher sur les premiers traitements capables de freiner le développement de ces pathologies.
Notre service d’évaluation de l’efficacité de molécules actives est basé sur un savoir-faire unique dans la production et la stabilisation des oligomères à partir de monomères humains. Chaque lot d’oligomère produit est identifié, et sa composition et sa toxicité sont évaluées avant d’être utilisées dans vos études.
Tous nos tests ont été rigoureusement validés, démontrant la reproductibilité et la fiabilité des situations expérimentales proposées.
Exemple de caractérisation
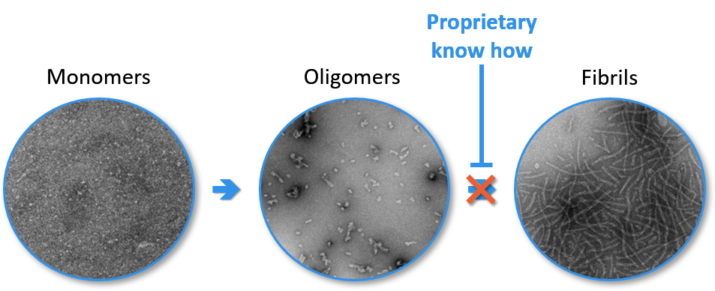
Coomassie blue staining of a Aβ 1-42 oligomers preparation in SDS-PAGE
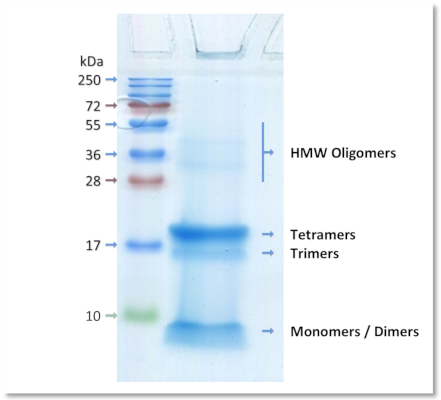
Dot-blot detection of Aβ 1-42 oligomers
Les préparations oligomères humains Aβ 1-42 ont été séparées à l’aide d’un gel SDS-PAGE à 15% en conditions non-réductrices. Le profil de gel révélé par la coloration au bleu de Coomassie démontre que les oligomères contiennent un mélange de dimères, de trimères et de tétramères stables, ainsi que des traces d’oligomères de haut poids moléculaire.
La présence d’oligomères Aβ1-42 a été mis en évidence avec l’anticorps Anti-oligomères A11(Lapin), qui reconnaît tous les types d’oligomères, sans interagir avec les fibrilles d’Aβ1-42.
Our models
Alzheimer's disease
In vitro Amyloid-beta oligomers model
Ce modèle, basé sur nos préparations d’oligomères d’Aβ1-42 (AβO), permet la détection in vitro l’activité de molécules neuroprotectrice ou destinées à l’immunothérapie pour la maladie d’Alzheimer. Ces tests peuvent être réalisés en prétraitement (avant l’ajout de AβO) ou en co-incubation avec des cultures primaires de neurones corticaux de rats ou de souris.
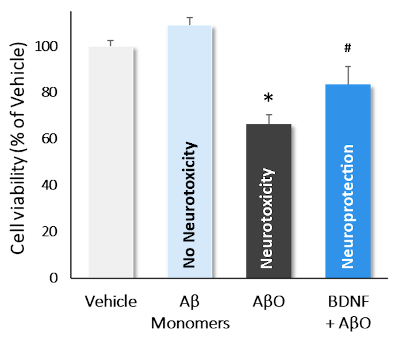
Incubation de neurones corticaux avec des monomères Aβ, AβO et AβO+BDNF. Les AβO ont diminué de manière significative la viabilité cellulaire (*; p<0,01*; p<0,01), tandis que les monomères n’ont montré aucun effet neurotoxique. L’incubation avec le BDNF a significativement inversé la neurotoxicité induite par les AβO (# ; p<0.01). Les données sont exprimées en pourcentage du véhicule (fixé à 100 % ; moyenne ± Ecartype (N=3, n=12)).
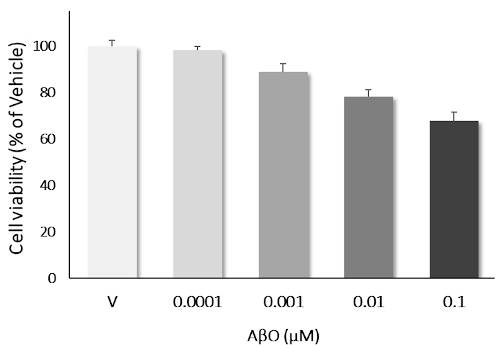
Les AβO induisent une neurotoxicité dose-dépendante : La mise en présence des neurones corticaux primaires avec une gamme de concentration croissante de AβO (0,1 nM à 0,1 μM) a montré une neurotoxicité dose-dépendante marquée. Les données sont exprimées en pourcentage du véhicule (fixé à 100 % ; moyenne ± Ecartype (N=3, n=12)).
In vivo Amyloid-beta oligomers model
Cette section est en construction.
Vous trouverez d’avantage d’informations dans notre dernière newsletter et au sein de notre dernier poster.
Parkinson's disease
In vitro alpha-synuclein oligomers model
Ce modèle, utilisant notre préparation d’oligomères d’alpha-synucléine (ASO), permet de détecter l’activité de molécules in vitro à des fins de neuroprotection ou d’immunothérapie pour le traitement la maladie de Parkinson. Ces tests peuvent être effectués en pré-traitement (avant l’ajout d’ASO) ou en co-incubation sur des cultures primaires de neurones mésencéphaliques de rats ou de souris.
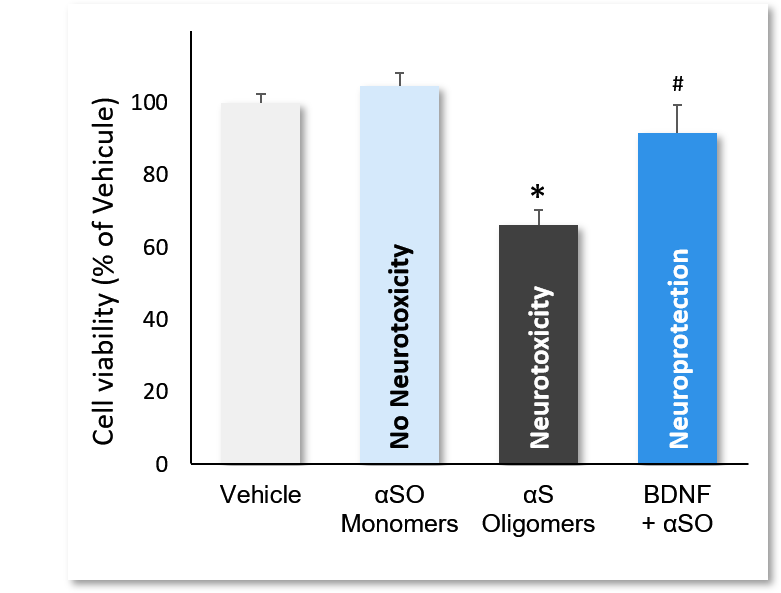
Incubation de neurones mésencéphaliques avec des monomères αS, αSO et αSO+BDNF. Les αSO ont diminué de manière significative la viabilité cellulaire (*; p<0,01), tandis que les monomères n’ont montré aucun effet neurotoxique. L’incubation avec le BDNF a significativement inversé la neurotoxicité induite par l’ASO (#; p<0.01). Les données sont exprimées en pourcentage du véhicule (fixé à 100 % : moyenne ± écartype (N=3, n=12).
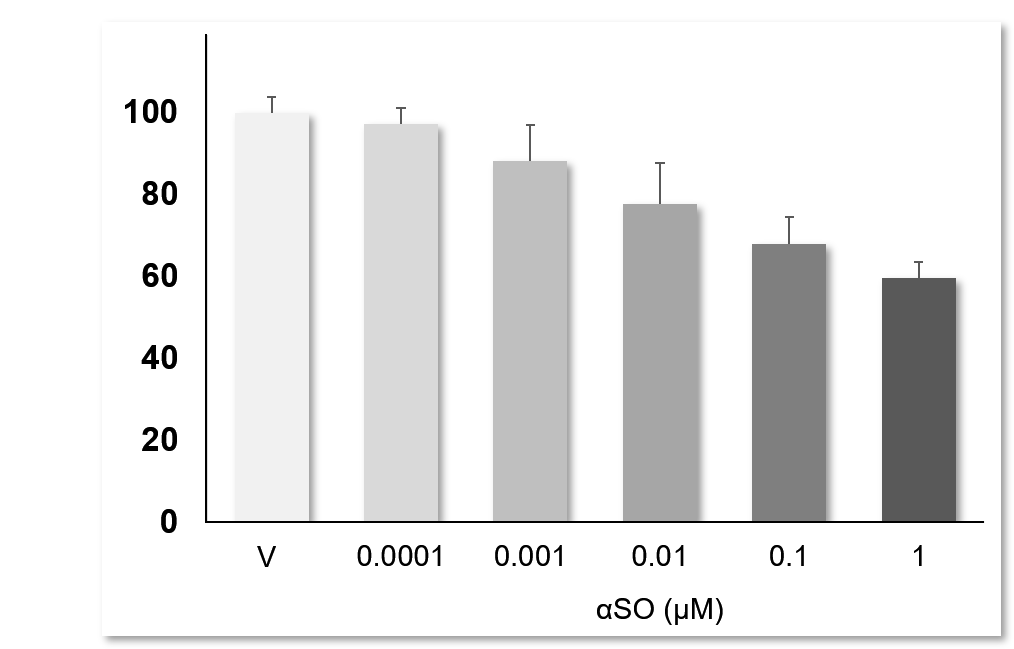
Les αSO induisent une neurotoxicité dose-dépendante : La mise en présence des neurones mésencéphaliques primaires avec une gamme de concentration croissante de αSO (0,1 nM à 0,1 μM) a montré une neurotoxicité dose-dépendante marquée. Les données sont exprimées en pourcentage du véhicule (fixé à 100 % ; moyenne ± Ecartype (N=3, n=12)).





